Норма носовой кости в 18 недель беременности
Содержание статьи
Оценка носовой кости в I триместре беременности: как, где, когда и зачем мы делаем

УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Задача пренатального скрининга — выявление беременных женщин группы высокого риска по рождению детей с хромосомными болезнями и врожденными пороками развития с целью более детального анализа состояния плода с помощью специальных методов [1].
С конца прошлого века в алгоритм пренатального скрининга включен расчет индивидуального комбинированного риска, центральное место в котором занимают ультразвуковой и биохимический скрининг в I триместре (11-14 нед беременности). Были созданы компьютерные программы расчета риска, учитывающие возраст, ультразвуковой маркер I триместра (толщина воротникового пространства — ТВП) и биохимические маркеры крови (β-hCG и PAPP-A) беременной женщины [2].
За последние 10 лет данная система полностью оправдала себя и получила дальнейшее развитие, путем прибавления к расчету риска добавочных ультразвуковых маркеров (оценка носовой кости, венозного протока, трикуспидальной регургитации, некоторых маркерных врожденных пороков развития). Расширение протокола осмотра с оценкой новых ультразвуковых маркеров (оценка носовой кости, кровоток в венозном протоке и на трикуспидальном клапане) улучшает чувствительность комбинированного скрининга благодаря увеличению частоты обнаружения и уменьшению частоты ложноположительных результатов [3].
Однако их оценка требует соответствующего углубленного обучения врача УЗД и получение сертификата компетентности на проведение данного вида исследования, так как только после получения доступа на конкретный вид исследования программа расчета риска будет учитывать эти данные в своих расчетах [1-3].
Преимуществами проведения УЗИ в 11-14 нед помимо установки точного срока беременности являются: ранняя диагностика многих пороков развития плода, оценка маркеров хромосомных аномалий для выявления беременных высокого риска по хромосомным аномалиям у плода, при многоплодной беременности именно в ранний срок возможно установить хориальность, что является важнейшим фактором, определяющим исход многоплодной беременности, возможность выявить женщин группы высокого риска по развитию преэклампсии в поздние сроки беременности [3, 4].
Копчико-теменной размер плода (КТР) для проведения скрининга I триместра должен быть в пределах 45-84 мм. Для оценки носовой кости в I триместре беременности необходимо соблюдать строгие условия. Это адекватное увеличение (на снимке должны быть только голова и верхняя часть грудной клетки), среднесагиттальный скан (должны быть визуализированы эхогенный кончик носа, небный отросток верхней челюсти, диэнцефалон), нос представлен тремя «К» (кончик носа, кожа, кость). Кожные покровы и кости носа визуализируются в виде знака «равенства», нос параллелен датчику.
Такие правила, как размер плода, адекватное увеличение, среднесагиттальный скан идентичны таковым при измерении ТВП. Таким образом, при выведении корректного скана для измерения ТВП, что является обязательным при проведении УЗ-исследования в сроки 11-14 нед беременности, оценка носовой кости проводится в том же самом срезе, не требуя получения дополнительных изображений.
Если все критерии соблюдены, то на уровне носа плода должны быть видны три четко различимые линии: верхняя линия представляет собой кожу, книзу от нее визуализируется более толстая и более эхогенная, чем кожа носовая кость. Третья линия, визуализируемая кпереди от носовой кости и на более высоком уровне, чем кожа — это кончик носа (рис. 1).
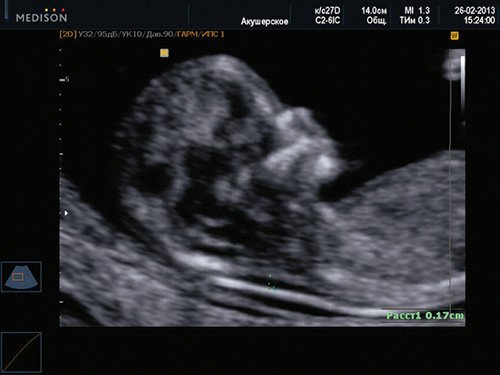
Рис. 1. Нормальная носовая кость.
Считается, что носовая кость нормальна, когда она по своей структуре более эхогенна, чем надлежащая кожа и патологична, если она не видна (аплазия) (рис. 2) или ее длина меньше нормы (гипоплазия) (рис. 3). В случае одинаковой или меньшей эхогенности носовой кости чем кожи носовая кость считается патологической (рис. 4).
Рис. 2. Аплазия носовой кости.
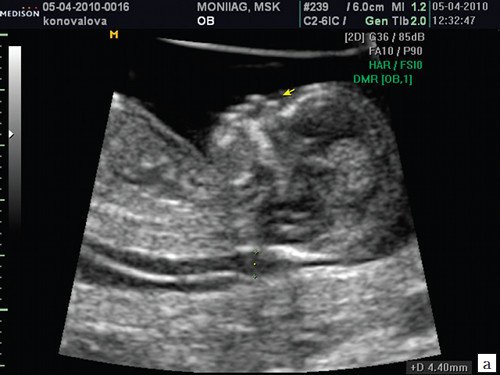
а) Стрелкой указана эхогенная кожа плода.
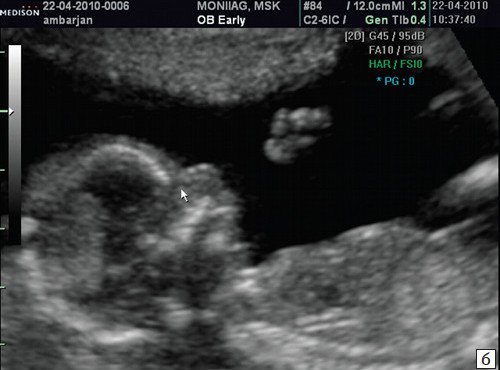
б) Стрелкой указано отсутствие носовой кости.
Рис. 3. Гипоплазия носовой кости.
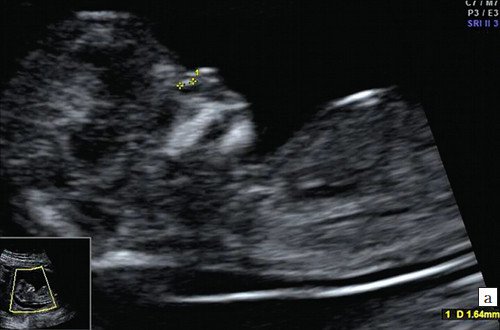
а) Носовая кость в 12 нед и 2 дня длиной 1,4 мм (меньше нижней границы нормы).
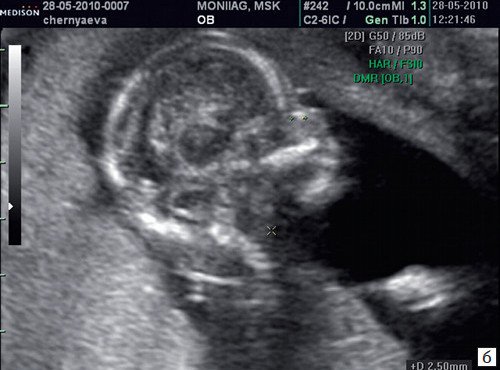
б) Носовая кость 2,1 мм в 14 нед у плода с синдромом Дауна.
Рис. 4. Патология носовой кости
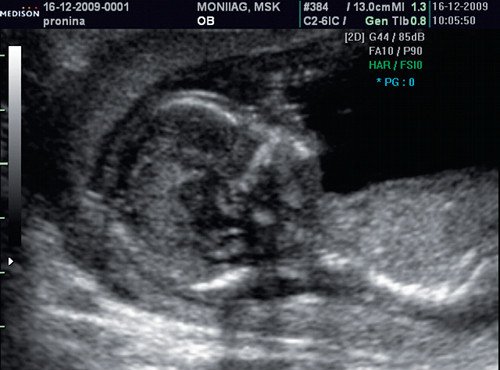
Рис. 4. Сниженная эхогенность носовой кости.
Итак, патологией носовой кости считается:
- отсутствие носовой кости (аплазия);
- изменение ее длины (гипоплазия);
- изменение ее эхогенности.
Учитывая то, что многие работы по изучению этого важного маркера были проведены на различных по составу группах населения, данные по частоте отсутствия носовой кости у разных авторов отличаются. Так, по усредненным данным по мультицентровым исследованиям FMF в 11-14 нед носовая кость отсутствует у эуплоидов (в случае нормального кариотипа) от 1 до 2,6% плодов [2, 5, 6], при хромосомных патологиях: у плодов с трисомией 21 — в 60%, с трисомией 18 — в 50%, у плодов с трисомией 13 — у 40% [3].
Проводились многочисленные работы, посвященные измерению и оценке носовой кости в срок 11-14 нед беременности. Некоторые авторы предлагают оценивать лишь ее наличие или отсутствие (+/-) [7]. Некоторые работы кроме оценки носовой кости посвящены ее измерению, сравнивая длину с нормативными для данного срока значениями [8-10].
Эволюция развития оценки этого маркера и мнение специалистов на этот счет, пожалуй, одна из самых дискутабельных проблем, не до конца решенных в скрининге I триместра беременности. Большинство авторов считают оценку носовой кости в I триместре одной из самых сложных задач среди всех остальных маркеров. И это мнение не лишено оснований.
Безусловно, сторонники теории о том, что для каждой расы (азиаты, афро-американцы и т.д.) и популяции народов (буряты, калмыки, народы Северного Кавказа) должны существовать свои процентильные нормативы для каждого КТР правы. Однако проведение этих исследований возможно лишь тогда, когда в рамках безвыборочного скрининга на нормальных плодах будут проведены мультицентровые исследования с измерением носовой кости.
В программе расчета риска Astraia при оценке носовой кости есть 4 поля: норма, патология (аплазия/гипоплазия), четко не видна, оценить не удалось, т.е. для того, чтобы поставить диагноз «Гипоплазия носовой кости» нужно удостовериться, что она на самом деле меньше нормативных значений для данного срока беременности, а это можно сделать только путем ее измерения и сравнения с известным нормативом.
Метод оценки носовой кости только лишь «да/нет», когда предлагается только увидеть носовую кость и сравнить ее эхогенность с кожей весьма «аппаратозависим», т.е. очень вариабелен и зависит от технических настроек ультразвукового сканера. При получении «жесткого» изображения, характерного для некоторых ультразвуковых аппаратов со специфическими заводскими пресетами (настройками) для осмотра плода в I триместре, всегда эхогенность кожи будет сопоставима, т. е. одинакова с эхогенностью носовой кости. Таким образом, у врачей практического звена, не имеющих возможности работать на сканерах премиум класса, возникают объективные трудности с оценкой этого важного дополнительного диагностического маркера.
Как сторонники метода измерения носовой кости в 11-14 нед приведем данные по Московской области. Область является разнородной по населяющему ее национальному составу. В своей работе мы пользовались нормативными значениями длины носовой кости, опубликованными J. Sonek и соавт. в 2003 году [8], за нижнюю границу нормы принимая значение 5-го процентиля (таблица).
Таблица. Нормативы длины носовой кости (НК) в срок 11-14 недель.
| Срок, недель | 11 | 12 | 13 | 14 |
|---|---|---|---|---|
| Длина НК, мм | 1,4 | 1,8 | 2,3 | 2,5 |
Экспертами окружных кабинетов Московской области проводилась оценка не только присутствия и отсутствия носовой кости, но и ее измерение у всех беременных женщин (около 150 тысяч обследованных за 3,5 года работы скрининга). Все 31 эксперт Московской области имеют действующий сертификат компетенции FMF как на ТВП, так и на оценку носовой кости. Проведенный анализ выявления патологии (аплазия/гипоплазия) носовой кости у плодов с хромосомной патологией показал, что из пренатально выявленных 266 случаев синдрома Дауна у плода в I триместре носовая кость была патологична в 248 случаях, что составляет 93,2%.
Это высокая частота патологии носовой кости при синдроме Дауна свидетельствует о правильно выбранном алгоритме оценки носовой кости от которого мы никогда не намерены отказываться, получая такие высокочувствительные результаты, особенно, что касается диагностики синдрома Дауна. В случаях выявления других хромасомных аномалий, частота выявления патологии носовой кости была сопоставима с данными литературы. При синдроме Эдвардса носовая кость патологична у 78 плодов, что составляет 71%, при синдроме Патау — у 24 (59%) плодов, при моносомии Х — в 24 (42%) случаях, при триплоидии — у 22 (49%) плодов.
Особо хотелось бы подчеркнуть, что в нашем исследовании было 10 беременных корейской национальности, попавших в группу риска по хромосомной патологии. У 4 из них была диагностирована патология носовой кости у плода. Можно было ожидать, что это этническая особенность, однако все данные плоды при пренатальном кариотипировании имели хромосомную патологию (трисомию 21). И, наоборот, у 6 плодов, имеющих нормальный кариотип как по длине, так и по эхогенности носовой кости были в пределах нормативных для данного срока значений.
В работах некоторых авторов установлено, что при трисомии 21 в I триместре беременности лишь у 25% плодов носовая кость отсутствовала, в более высокой частоте она была гипоплазирована (36%) [11].
Так как у нормальных плодов отсутствие носовой кости более характерно для срока 11 нед беременности, чем 13 нед, FMF дает практическую рекомендацию о том, что если в этот срок (11 — начало 12 нед) у плода отсутствует носовая кость при условии нормальных показателей других маркеров (ультразвуковых и биохимических) не стоит учитывать этот показатель при расчете индивидуального риска. В дальнейшем рекомендуется провести дополнительное ультразвуковое исследование через одну неделю. В том случае, если носовая кость останется патологична, необходимо учитывать этот факт при перерасчете величины индивидуального риска по хромосомным аномалиям [4].
Оценка носовой кости улучшает результаты комбинированного скрининга. Частота обнаружения патологии увеличивается с 90 до 93%. Частота ложноположительных результатов уменьшается с 3,0 до 2,5% [2, 3, 5, 6].
Таким образом, собственные данные позволяют нам рекомендовать оценивать носовую кость в сроки 11-14 нед по двум параметрам: эхогенность и длина, принимая за патологию носовой кости ее отсутствие, гипоплазию и снижение эхогенности.
Литература
- Баранов В.С., Кузнецова Т.В., Кащеева Т.К. и др. Современные алгоритмы и новые возможности пренатальной диагностики наследственных и врожденных заболеваний. Методические рекомендации. С.-Петербург, 2013. С. 23-46.
- Nicolaides K.H. Screening for fetal aneuploidies at 11-13 weeks//Prenatal diagnosis. 2011, 31: 7-15.
- Nicolaides K.H. Пер. с англ. Михайлова А., Некрасовой Е. Ультразвуковое исследование в 11-13+6 недель беременности. С.-Петербург, 2007. ИД «Петрополис», 142 с.
- https://www.fetalmedicine.org/the-11-13-weeks-scan
- Kagan K.O., Cicero S., Staboulidou I., Wright D., Nicolaides K.H. Fetal nasal bone in screening for trisomies 21, 18 and 13 and Turner syndrome at 11-13 weeks of gestation // Ultrasound Obstet Gynecol. 2009; 33: 259-264.
- Kagan K.O., Staboulidou I., Cruz J., Wright D., Nicoladides K.H. Two-stage first-trimester screening for trisomy 21 by ultrasound assessment and biochemical testing // Ultrasound Obstet Gynecol. 2010. V. 36. N 5. P. 542-547.
- Cicero S., Curcio P., Papageorghiou A., Sonek J., Nicolaides K. Absence of nasal bone in fetuses with trisomy 21 at 11-14 weeks of gestation: an observational study // Lancet 2001; 358:1665-1667.
- Sonek J.D., Mckenna D.,Webb D.,Croom C., Nicolaides K. Nasal bone length throughout gestation: normal ranges based on 3537 fetal ultrasound measurements // Ultrasound in Obstetrics & Gynecology. 2003. V. 21. N 2. P. 152-155.
- Kanellopoulos V., Katsetos C., Economides D.L. Examination of fetal nasal bone and repeatability of measurement in early pregnancy // Ultrasound Obstet Gynecol. 2003 Aug;22(2):131-4.
- Cicero S., Bindra R., Rembouskos G., Tripsanas C., Nicolaides K.H. Fetal nasal bone length in chromosomally normal and abnormal fetuses at 11-14 weeks of gestation // Matern Fetal Neonatal Med. 2002; 11: 400-402.
- Keeling J.W., Hansen B.F., Kjaer I. Pattern of malformations in the axial skeleton in human trisomy 21 fetuses // Am J Med Genet. 1997; 68: 466-471.

УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Источник
Ультразвуковой скрининг второго триместра
Ультразвуковой скрининг второго триместра проводится на сроках 19-21 неделя беременности и его основными задачами являются:
1) оценка фетометрических параметров для определения их соответствия менструальному сроку беременности и исключения задержки внутриутробного развития плода;
2) оценка ультразвуковой анатомии плода с целью дородовой диагностики врожденных пороков развития (ВПР) и других патологических состояний;
2) формирование среди беременных группы риска, угрожаемой по рождению детей с хромосомными аномалиями и другими врожденными и наследственными заболеваниями, путем выявления эхографических маркеров этих заболеваний;
3) изучение особенностей развития плаценты и других провизорных органов, а также оценка количества околоплодных вод с целью получения дополнительной информации о развитии и течении беременности.
Довольно часто происходит путаница в связи с тем, что существует ещё и биохимический скрининг второго триместра, но у этих двух скринингов различные задачи и сроки проведения. Биохимический скрининг (тройной, четверной тест) проводится на сроках 14-20 недель беременности (рекомендованные сроки 16-18 недель) и подразумевает под собой исследование крови беременной с целью оценки риска некоторых хромосомных аномалий, дефекта нервной трубки, а также вероятности развития плацентарной недостаточности. Для расчёта рисков используются данные ультразвукового исследования, выполненного во время скрининга первого триместра в 11-13 недель.
Сроки проведения УЗ исследования во время беременности оказывают серьёзное влияние на качество дородового обследования. С одной стороны, срок исследования должен определяться оптимальной визуализацией внутренних органов плода с целью максимально точной диагностики врождённых пороков развития (ВПР). С другой стороны, он регламентируется возможностью прерывания беременности по медицинским показаниям в тех случаях, когда выявляются инвалидизирующие или несовместимые с жизнью ВПР.
Несомненно, в 22-24 недели оценка внутренних органов плода с помощью УЗ представляет меньшие трудности, чем в 19 недель, но в нашей стране рекомендуемые сроки для прерывания беременности по медицинским показаниям ограничены сроком 22-23 недели.
В связи с этим, определённым компромиссом мне, как врачу УЗД, представляется срок 20-21 неделя. Но многие акушеры-гинекологи стремятся отправить беременную женщину на УЗИ как можно раньше, желательно уже в 18-19 недель. Конечно, на этом сроке уже можно исключить большинство серьёзных пороков. Но многими исследованиями было доказано, что оптимальными сроками для проведения второго скринингового ультразвукового исследования является интервал от 20 до 22 недель беременности. В эти сроки чёткая визуализация всех структур плода возможна в 90% случаев, тогда как в 18–19 недель – только в 76%.
Несмотря на повсеместное распространение ультразвуковых исследований, дородовая диагностика ВПР продолжает вызывать трудности. По данным многочисленных зарубежных исследований, проведенных в разные годы, показатель их выявляемости в среднем составляет 45%. Российское мультицентровое исследование продемонстрировало аналогичный результат – 55%. Таким образом, можно сделать неутешительный вывод о том, что при скрининговых исследованиях каждый второй ВПР, подлежащий ультразвуковой диагностике, в условиях практического здравоохранения пропускается и констатируется только после рождения ребенка. Очевидно, что средние показатели отражают лишь тенденции в ультразвуковой диагностике и не характеризуют работу каждого специалиста. В разных клиниках чувствительность эхографии в отношении ВПР варьирует в очень широких пределах – от 20 до 97%.
Эффективность как скрининговых, так и селективных ультразвуковых исследований зависит от многих факторов, главными из которых являются:
1) квалификация врачей ультразвуковой диагностики;
2) сроки проведения и количество исследований;
2) диагностические возможности ультразвукового оборудования.
Оценка фетометрических параметров
Чтобы понять, большой ребёнок или маленький для данного конкретного срока, худенький или толстенький, нет ли отставания длины конечностей, а также их искривления и деформации с целью исключения различных скелетных аномалий, проводится, т.н. фетометрия. В процессе фетометрии производится измерение размеров головы, окружности живота, длины бедра, плечевой кости, предплечья и голени.
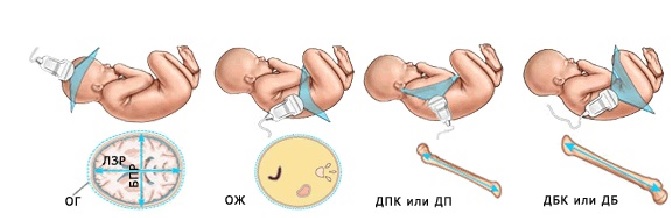
Кроме того оценивается длина носовых костей (ДНК) и отношение толщины преназальных тканей к ДНК. До срока 26 недель отношение ТПТ/ДНК > 0.8 является одним из маркеров хромосомных аномалий. В третьем триместре данный признак утрачивает своё значения из-за довольно выраженного преназального отёка у абсолютно здоровых детей. Очень часто, глядя на картинку своего малыша в 30 недель, мамы удивляются какой большой у ребёнка нос. На самом деле, нос чаще обычный, но кажется таким из-за отёка. А вот во втором триместре, в норме толщина преназальных тканей заметно меньше длины носовых костей.
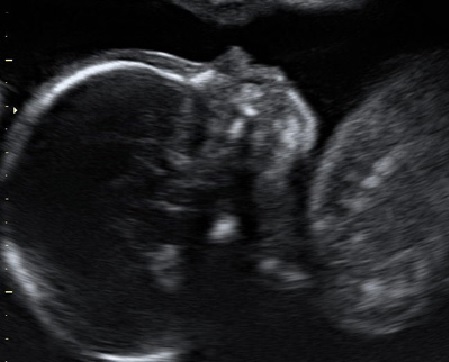
Данные фетометрических измерений, занесенные в протокол, дают возможность врачу судить о размерах плода и об их соответствии менструальному сроку беременности. Все полученные значения необходимо сравнивать со специально разработанными для данного региона нормативными показателями.
Следует помнить, что при регулярном менструальном цикле срок беременности рассчитывается от первого дня последней менструации. Категорически неправильно вносить поправки в срок беременности на основании полученных во 2 триместре фетометрических данных. Вольное обращение с установленным сроком беременности нередко приводит к несвоевременному выявлению задержки внутриутробного развития плода и к другим серьезным диагностическим ошибкам.
Оценка ультразвуковой анатомии плода
Изучение анатомии плода включает последовательный осмотр структур головного мозга, лица, позвоночника, лёгких, сердца и главных сосудов, органов брюшной полости, почек, мочевого пузыря, наружных половых органов и конечностей.
Однако следует отметить, что даже самое тщательное исследование во 2 триместре не позволяет полностью исключить все пороки развития, поскольку некоторые нозологические формы проявляют себя только в поздние сроки беременности.
В рамках данной статьи я конечно не стану рассказывать о тех многочисленных возможных изменениях анатомии плода, которые могут быть выявлены во время УЗИ во 2 триместре. Расскажу только о тех особенностях развития ребёнка, которые отдельно отмечаются в заключении, описываются в протоколе и без должного объяснения, как правило, вызывают тревогу и беспокойство родителей, но при этом совершенно не являются пороком развития.
Первая такая особенность — это кисты сосудистых сплетений (КСС) боковых желудочков головного мозга. Они могут быть единичными и множественными, одно- и двухсторонними. Обычно КСС возникают между 13 и 18 неделями беременности, когда в сосудистой оболочке появляется сетчатая структура (свободное пространство, заполненное жидкостью). Постепенно эти пространства между сосудистыми ворсинками уменьшается и «кисты» исчезают. В исследованиях было показано, что до 20 недель КСС регистрируются в 59.5% случаев, в 20-24 недели – примерно в 35%, после 24 недель в 5 % наблюдений. К началу III триместра беременности подавляющее большинство (98%) КСС исчезают. Изолированные КСС являются доброкачественными изменениями, не влияющими на прогноз для жизни и здоровья.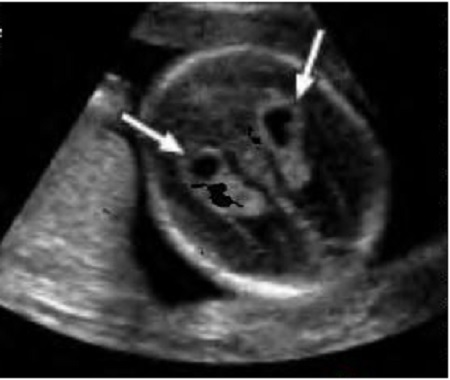
Второй особенностью развития является гиперэхогенный фокус (ГЭФ) в сердце плода. Выглядит это как подвижная белая точка в полости правого или левого желудочка. В зарубежной литературе его эхографическую картину сравнивают с мячиком для гольфа. Объясняется появление такого фокуса избыточным отложением солей кальция в одной из сосочковых мышц клапанного аппарата сердца. Примерно у 5% здоровых детей во время скрининга 2 триместра будет выявлен такой фокус. Повышенное внимание к этой находке долгое время было связано с тем, что ГЭФ встречается у 20% плодов с синдромом Дауна. Но если у вашего ребёнка не было найдено других маркеров ХА, то ГЭФ, как изолированная находка, не является поводом для беспокойства, не ассоциирован с пороками сердца и не требует дополнительного обследования и наблюдения. Во время УЗИ в 30 недель эта гиперэхогенная точка обычно уже не видна.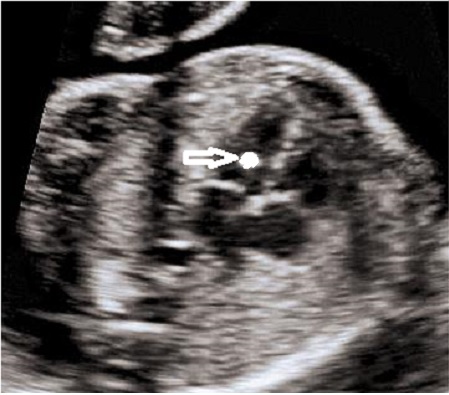
Ещё одно довольно частое заключение, которое в большинстве случаев не повлечёт за собой никаких последствий кроме наблюдения – это пиелоэктазия – расширение почечной лоханки от 4 до 10мм. Такое расширение чаще всего бывает транзиторным и не требует лечения. В случае если вам в заключении написали пиелоэктазия, а в описании почек указали, что отмечается расширение лоханок, скажем до 5-7мм, а это бывает совсем не редко, причём у мальчиков в 3 раза чаще, чем у девочек — не нужно пугаться. В большинстве случаев, в 30-32 недели эти цифры останутся примерно такими же или уменьшаться и никакого лечения или специального наблюдения не потребуется. 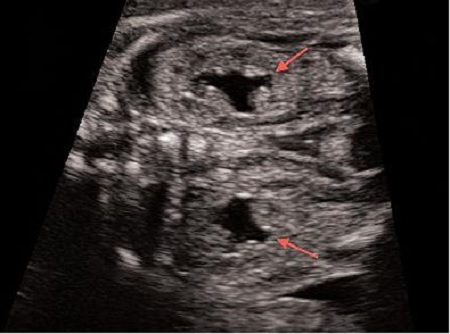
Но в редких случаях, в динамике происходит увеличение передне-заднего размера почечной лоханки более 10мм. Расширение почечной лоханки более чем 10 мм — это уже состояние, которое потребует консультации нефролога и медицинского вмешательства после рождения ребёнка. Эта патология мочевыделительной системы называется гидронефроз — прогрессирующее расширение лоханки и чашечек, возникающее вследствие нарушения оттока мочи в области лоханочно-мочеточникового сегмента, что в конечном итоге приводит к необратимым изменениям в паренхиме и прогрессивному снижению функции почек.
Формирование среди беременных группы риска, угрожаемой по рождению детей с хромосомными аномалиями на самом деле является следствием оценки анатомии плода и фетометрии. Каждый из выявляемых пороков развития в той или иной степени ассоциирован с хромосомными аномалиями, только какие-то в большей степени, какие-то в меньшей. В связи с этим, очень часто при обнаружении какого-то порока, и всегда при обнаружении сочетанных пороков, в первую очередь рекомендуется пренатальное консультирование и кариотипирование плода.
Пожалуй, задержусь на этом слове «рекомендуется». Не редко в интернете можно найти статьи примерно с таким заголовком: «Пренатальная диагностика: уничтожение больных детей до рождения». Никто не будет заставлять или принуждает Вас к тому, что Вы не хотите делать. Но имея максимально полную информацию о данном конкретном заболевании, о возможностях современной медицины исправить имеющиеся нарушения, о качестве и продолжительности жизни ребёнка после всех оперативных вмешательств – Вы сможете принять осознанное и взвешенное решение. Цель пренатальной диагностики и консультирования — не уничтожение, а информирование родителей о наличии и/или вероятности возможных проблем у ещё нерождённого ребёнка!
Изучение особенностей развития плаценты, других провизорных органов и количества околоплодных вод
Роль плаценты как органа, обеспечивающего формирование и рост плода, чрезвычайно велика как при физиологической беременности, так и при осложненном ее течении. Строение и функции плаценты непостоянны. Они меняются с увеличением срока беременности, что связано с возрастающими потребностями развивающегося плода и в значительной мере обусловлено состоянием маточно-плацентарного кровообращения. В настоящее время не вызывает сомнений тот факт, что полноценное развитие плода во многом определено адекватной маточно-плацентарной гемодинамикой, которая, в свою очередь, зависит от анатомо-морфологических особенностей плаценты.
С внедрением в клиническую практику ультразвукового метода исследования появилась возможность получения информации о локализации, размерах и структуре плаценты.
Локализация плаценты
Плацента может определяться по передней или задней стенке матки, по правому или левому ребру, ближе к дну или к нижнему сегменту. На развитие ребёнка расположение плаценты влияния не оказывает. Исключением является «предлежание плаценты», когда она перекрывает своим краем внутренний зев. Наличие плацентарной ткани в области внутреннего зева шейки матки может приводить к кровотечениям, иногда очень выраженным, поэтому требует определённых ограничений в плане образа жизни, физических нагрузок, возможности перелётов и дальних поездок. Методом родоразрешения при предлежании плаценты является кесарево сечение. 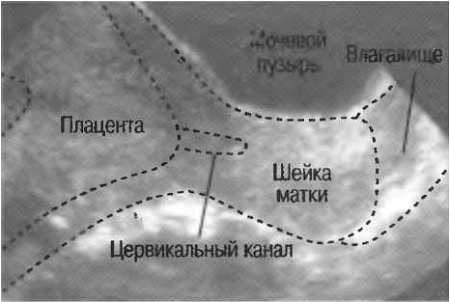
Кроме того выделяют «низкую плацентацию», когда расстояние между внутренним зевом и краем плаценты менее 3см во 2 триместре и менее 5см в 3 триместре. Однако доказано, что около 95% низко расположенных во II триместре плацент «поднимается» к концу беременности.
Размеры и эхоструктура плаценты отличаются очень большим разнообразием и большинство исследователей сходятся во мнении, что то, как плацента выглядит на эхограмме, не отражает её функциональных возможностей. Другими словами, исследователи лишены возможности мгновенно оценивать морфологическую структуру плаценты и особенно ее измененных с точки зрения эхографии участков. Следовательно, в повседневной практике врачам ультразвуковой диагностики приходится оценивать ультразвуковую картину плаценты весьма субъективно. Поэтому, если размеры плода соответствуют гестационному сроку, по данным допплерометрии нет нарушений гемодинамики в системе мать-плацента-плод и речь не идёт о возможной резус –сенсибилизации, то в большинстве случаев и нет причин для волнения
Ультразвуковая оценка пуповины должна включать изучение:
1) места прикрепления пуповины к плаценте;
2) места прикрепления пуповины к передней брюшной стенке плода;
3) количества сосудов пуповины;
4) патологических изменений пуповины.
Каждый из этих пунктов может включать целый ряд нарушений, влияющих на развитие ребёнка, риски развития ВЗРП и антенатальной гибели плода, а также выраженных, угрожающих жизни матери и плода кровотечений во время родов. Кроме того во время УЗИ возможно заподозрить наличие истинного узла пуповины, что также представляет определённую угрозу для состояния плода во время естественных родов и может склонить чашу весов в пользу родоразрешения путём операции кесарево сечение.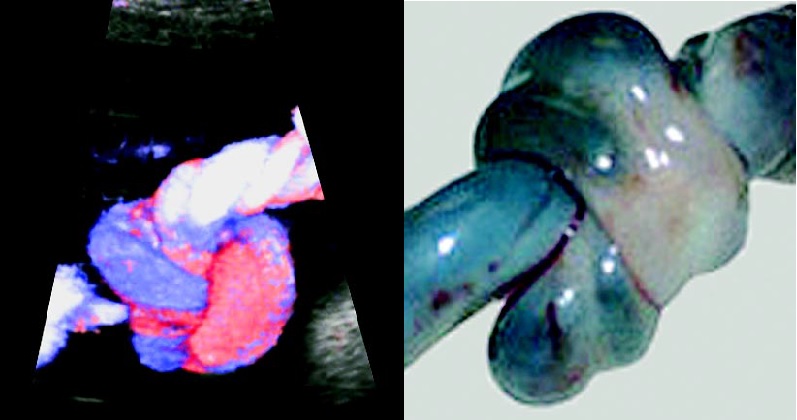
Обвитие пуповины, выявленное во 2 триместре, не является патологическим состоянием и не требует дополнительного наблюдения.
Околоплодные воды – сложная, биологически активная среда, обеспечивающая нормальную жизнедеятельность плода.
Единственной на сегодня обязательной ультразвуковой характеристикой околоплодных вод является их количество. Наибольшее распространение в клинической практике получил метод измерения вертикального размера свободного кармана околоплодных вод, а также вычисление индекса амниотической жидкости (ИАЖ).
Существует множество причин, приводящих к маловодию. К наиболее частым относятся обструкция мочевыводящих путей со вторичным поражением паренхимы почек, агенезия почек плода, патология плаценты, подтекание вод, ХА и некоторые другие.
Причины многоводия до конца не изучены и ассоциированы с большим разнообразием аномалий развития плода и состояний будущей мамы. В случае, когда каких-либо отклонений в развитии ребёнка, а также заболеваний со стороны матери выявить не удаётся, говорят об «идиопатическом многоводии»
Как видите, ультразвуковой скрининг 2 триместра является очень важным исследованием, которое рекомендовано всем беременным на сроке 19-21 неделя. Позволяющим выявить/заподозрить или исключить большое количество различных состояний влияющих на дальнейшее развитие ребёнка, течение беременности и родов, а также своевременно принять меры, значительно снижающие уровень перинатальной/ материнской заболеваемости и смертности.
Здоровья вам и вашим малышам!
Использованная литература:
Основы УЗ скрининга в 20-22 недели М.В. Медведев
Пренатальная эхография М.В. Медведев
Нормальная ультразвуковая анатомия плода М.В. Медведев, Н.А. Алтынник
Источник